Ikatan Kimia
Kestabilan Unsur
Unsur-unsur di alam cenderung stabil. Kesetabilan unsur bisa diperoleh jika jumlah elektron pada kulit terluarnya (elektron valensi) sama dengan jumlah yang dimiliki gas mulia, yaitu sebanyak 8 elektron /oktet dan 2 elektron /duplet. Kita tahu bahwa gas mulia adalah merupakan unsur yang paling tidak reaktif (kestabilan tinggi).
Agar seperti gas mulia, maka unsur-unsur bekerja sama satu dengan yang lain sehingga terjadi gaya tarik menarik antar atom. Gaya tarik menarik antar atom dalam suatu zat itulah yang dinamakan ikatan kimia.
cara suatu atom untuk mencapai kestabilan mencapai seperti gas mulia, yaitu :
1. Dengan cara melepaskan elektron, sehingga bermuatan positip sebesar sejumlah elektron yang dilepaskan (menurut Walter Kossel).
Contoh : 12Mg à 12Mg2+ + 2e–
kalau kita perhatikan dari struktur elektronnya :
12Mg : 2 , 8 , 2 (tidak stabil)
12Mg2+ : 2 , 8 , 0 (stabil,seperti Ne)
2. Dengan cara menarik elektron, sehingga menjadi bermuatan negatif sebesar jumlah elektron yang diterimanya (menurut Walter Kossel).
Contoh : 9F + e- à F-1
Kalau kita lihat dari struktur elektronnya :
| 9F | : | 2, 7 (tak stabil) |
3. Dengan cara menggunakan pasangan elektron bersama. Ada 2 (dua) macam pasangan elektron yang digunakan bersama(menurut Lewis):
a. Masing-masing atom yang berkaitan menyumbangkan satu elektron.
Contoh :
Dalam molekul HCl
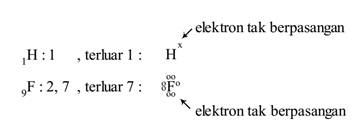
Elektron-elektron yang tidak berpasangan akan bergabung membentuk pasangan elektron yang digunakan bersama, sehingga atom H seakan punya 2 elektron (seperti He) sedang atom F seakan punya 8 elektron.
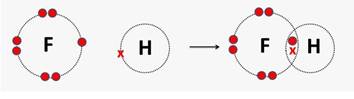
b. Pasangan elektron hanya berasal dari salah satu atom saja.
Contoh : Dalam Molekul NH4+
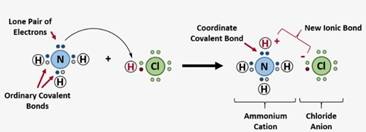
B. Macam-macam Ikatan Kimia
Atas dasar cara-cara untuk mencapai keadaan stabil di atas, maka dikenal ada 2 (dua) jenis ikatan yang utama:
1) Ikatan Ion
Ikatan ion disebut juga ikatan elektrovalen atau ikatan heteropolar. Ikatan ini terjadi akibat adanya gaya elektrostatis antara ion positif dan ion negatif. Ion-ion ini sendiri terjadi akibat serah terima elektron atom-atom yang berikatan.
Contoh :
11Na : 2, 8, 1 à Na+: 2, 8 (stabil)
17Cl : 2,7 à Cl-1 : 2, 8, 8 (stabil).
Elektron yang dilepaskan Na ditangkap Cl, sehingga Na+ akan berikatan dengan Cl-1 membentuk NaCl.
Ikatan ion biasanya terjadi unsur-unsur logam dengan unsur-unsur non logam.

2) Ikatan Kovalen
Ikatan kovalen terjadi akibat penggunaan pasangan elektron bersama. Ikatan ini biasanya terjadi antara unsur-unsur non logam dengan unsur-unsur non logam.
Ada tiga jenis ikatan kovalen, yaitu:
a. Ikatan Kovalen Non Polar
Ikatan ini terjadi jika atom - atom yang berikatan elektronegatifitasnya sama.
Contohnya : O2, H2, Cl2, N2.
Pada H2 masing-masing atom H mempunyai elektron terluar 1 (satu), sehingga masing-masing menyumbang satu elektron dan ikatannya tepat di tengah antara H dengan atom H yang satunya.
Molekul yang terbentuk dari ikatan kovalen dapat bersifat polar atau non-polar.
1) Molekul polar, bila ikatan antar atomnya bersifat polar dan bentuk molekulnya asimetris.
2) Molekul non-polar, bila:
ü Ikatan antar atomnya bersifat non-polar, Contoh : H – H ; O = O; Cl - Cl
ü Ikatan antar atomnya bersifat polar dan bentuk molekul simetris. Contoh : F-Be-F ; O=C=O

b. Ikatan Kovalen Polar.Terbentuk jika unsur-unsur yang berikatan mempunyai perbedaan elektronegatifitas ( ΔE > 0).
Contoh : HCl, H2O, NH3
Dalam molekul HCl, atom H mempunyai satu elektron valensi dan atom klor mempunyai tujuh elektron valensi terdiri tiga pasang elektron dan tak
berpasangan satu. Yang tidak berpasangan inilah yang akan berpasangan dengan satu elektron dari atom H membentuk ikatan kovalen. Namun karena
atom klor jauh lebih elektronegatif dari pada atom H, maka pasangan elektron ikatan ini akan tertarik ke arah atom klor. Akibatnya terjadilah dwi kutub
(Dipol) : yang didekati pasangan elektron kutub (-) dan yang dijauhi pasangan elektron kutub (+) :
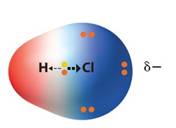
c. Ikatan Kovalen Koordinasi
Ikatan ini terbentuk jika pasangan elektron yang digunakan berasal dari salah satu atom saja. Sebagai contoh: antara H+ dengan H2O, antara BF3 dengan NH3, dan antara NH3 dengan H+.
Perhatikan pada BF3 dengan NH3
3) Perbedaan Sifat Fisik Senyawa Ion dan Kovalen
| Senyawa Ion | Senyawa Kovalen |
| sebagai larutan dapat | sebagai larutan umumnya
|
| membentuk kristal
| amorf |
| titik lebur dan titik didih yang relatif | umumnya titik lebur dan titik
|
| ikatannya sangat kuat | ikatannya relatif lemah |
4) Ikatan Logam
Ciri atom logam mempunyai sedikit elektron valensi dan banyak orbital kulit valensi. Untuk menjelaskan ikatan logam perlu dipertimbangkan data sifat-sifat
logam:
ü kemampuan menghantar listrik
ü kemampuan menghantar panas
ü mudah dibentuk (dapat ditempa dan dibuat kawat)
ü mempunyai kilap
ü elektropositif
Menurut teori lautan elektron (electron sea model)
Logam digambarkan sebagai jaringan ion positif yang berada dalam “lautan elektron” dan elektron-elektron ini bebas bergerak sehingga menyebabkan
timbulnya sifat-sifat logam di atas.
Makin kuat ikatannya makin tinggi titik leburnya, kekuatan ikatan logam ditentukan oleh banyaknya elektron valensi dari logam itu.
Contoh :
titik lebur Na < titik lebur Mg < titik lebur Al, hal ini dapat dijelaskan bahwa ikatan
logam Al > Mg > Na, hal ini disebabkan oleh jumlah elektron valensi Al > Mg > Na.
Kristal logam
Body Centered Cubic (BCC) BK = 8
Face Centered Cubic (FCC) BK = 12
Hexagonal Closed Packed (HCP) BK = 12
Catatan :
Bk = Bilangan koordinasi, yaitu banyaknya atom yang dapat mengelilingi atom pusat.
Struktur BBC lunak dapat diiris dengan pisau.
FCC kuat, liat HCP kerat, gampang patah.
C. Gaya antar Molekul
1. Ikatan van der Waals
Ikatan Van Der Waals terjadi karena adanya gaya tarik-menarik yang lemah antar molekul-molekul kovalen. Ikatan Van Der Waals dibangun oleh gaya-gaya sebagai berikut:
a. Gaya dipol-dipol/Gaya Orientasi
Terjadi antar molekul kovalen polar selain H dengan F, O, N.
Contoh : HCl, HBr, HI, H2S, H2Se
b. Gaya dipol-dipol Terimbas/Gaya Induksi
Terjadi antar molekul kovalen polar dengan kovalen non polar.
Contoh : H2O dengan O2
c. Gaya dipol sesaat-Dipol terimbas/Gaya London/Gaya Dispersi
Terjadi antar molekul kovalen non polar
Contoh : Br2; H2 (molekul diatomik)
CH4; CO2 (beda atom tapi simetris)
Hubungan Mr dan titik didih dengan kekuatan ikatan Van der Waals
Makin banyak jumlah elektron dalam molekul dan makin besar Mr nya, makin kuat ikatan Van der Waals dan makin tinggi titik didihnya.
Perhatikan hubungan jumlah elektron, Mr dan titik didih beberapa molekul berikut :
| Molekul | Σ elektron | Mr | Titik didih (°C) |
| H2 | 2 | 2 | - 253 |
Kuat lemahnya ikatan Van der Waals juga ada hubungannya dengan wujud zat.
Perhatikan pada senyawa halogen berikut :
| Senyawa | Mr | Titik didih (°C) | Wujud |
| F2 | 38 | -188 | gas |
2. Ikatan Hidrogen
Ikatan hidrogen adalah ikatan antar molekul yang sangat polar antara atom hidrogen (H) dengan atom lain yang mempunyai keelektronegatifan besar (seperti N, O dan F).
Contoh : ikatan antar molekul NH3, H2O, HF, alkohol (ROH) dan Asam karboksilat
(RCOOH) terutama yang jumlah atom C-nya kecil dan senyawa amina (RNH2).
Antar molekul NH3
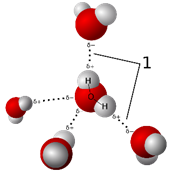
Pengaruh ikatan Hidrogen pada titik didih.
Titik didih suatu zat dipengaruhi oleh :
- kekuatan ikatan antar molekulnya, makin kuat ikatan antar molekulnya makin besar titik didihnya.
- massa molekul relatif (Mr) makin besar, makin besar pula titik didihnya.
Perhatikan hubungan Mr, beda keelektronegatifan dan titik didih senyawa golongan
halogen (VIIA).
| Senyawa | Mr | Beda | Titik didih |
| HF | 20 | 2,0 | +19 |
Dari HCl ke bawah Mr makin besar, titik didih makin besar, tetapi Mr. HF lebih kecil dibanding Mr HI, ternyata titik didih HF lebih besar. Hal itu disebabkan antar molekul HF membentuk ikatan hidrogen. Sedangkan HCl, HBr dan HI tidak membentuk ikatan hidrogen karena beda keelektronegatifannya relatif kecil.
Pada senyawa golongan oksigen (VIA)
| Senyawa | Mr | Beda | Titik didih |
| H2O | 18 | 1,4 | 100 |
Titik didih H2O besar karena antar molekul H2O membentuk ikatan hidrogen.
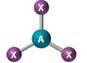
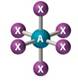
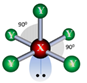
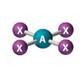
D. Bentuk Molekul
Cara VSEPR (Valency Shield Electron Pair Repulsion)
Teori ini menyatakan bahwa pasangan elektron dalam ikatan kimia ataupun pasangan elektron tidak dipakai bersama (pasangan elektron bebas) saling tolak menolak. Pasangan elektron cenderung untuk berjauhan satu sama lain. Urutan besarnya gaya tolakan sebagai berikut :
PEB – PEB > PEB – PET > PET – PET
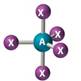
PEB = pasangan elektron bebas ® bernotasi E
PET = pasangan elektron terikat ® bernotasi X
Langkah-langkah untuk meramalkan bentuk molekul:
1) tentukan elektron valensi atom pusat (atom tunggal) ® notasi A.
2) tentukan elektron yang diperlukan oleh atom pengeliling untuk mencapai oktet/duplet
3) jumlahkan elektron-elektron pada pangkah 1, 2
4) menentukan bentuk geometris (ruang) dengan menghitung jumlah pasangan elektron
5) menentukan bentuk molekul dengan melihat jumlah ligan sesuai dengan pasangan elektron terikat (PET)
6) menentukan besar gaya tolakan (distorsi bentuk molekul) dengan menentukan PEB.
Contoh :
| CH4 | NH3 | H2O |
| atom pusat C = 4e
| atom pusat N = 5e | atom pusat O =8e |
Tabel geometri molekul sebagai fungsi sebaran geometris dari pasangan valensi
dan jumlah pasangan mandiri.
| pasangan | Notasi | Geometri | Polaritas |
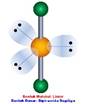
| 2 | AX2 |
| Non polar |
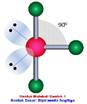
| 3 | AX3 |
| Non polar |
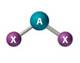
| AX2E |
| polar | |
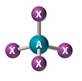
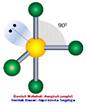
| 4 | AX4 |
| Non polar |
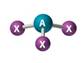
| AX3E |
| polar | |
| AX2E2 |
| polar | |
| 5 | AX5 |
| Non polar |
| AX4E |
| polar | |
| AX3E2 |
| polar | |
| AX2E3 |
| polar | |
| 6 | AX6 |
| Non polar |
| AX5E |
| polar | |
| AX4E2 |
| Non polar |
Cara Smart menentukan geometri molekul:
E = ( EV – X.n )/2
E = jumlah pasangan/domain elektron bebas
EV = jumlah elektron valensi atom pusat
X = jumlah domain elektron terikat
N = bila dikelilingi atom O, maka X dikali 2
Tentukan bentuk molekul dari:
a. H2O
EV = 6,
X = 2
E =(6 - 2) /2= 2
Tipe Molekul = AX2E2
BM = Planar bentuk V
b. SO3
EV = 6,
X = 3(2) = 6
E =(6 - 6)/2= 0
Tipe Molekul = AX3
BM = Segi tiga piramida
Soal latihan
1) Pada waktu membentuk ikatan, atom atom beberapa unsur cenderung mengikuti kaidah oktet. Hal ini dikemukakan oleh ...
A. Lavoisier
B. GN. Lewis dan Walter Kossel
C. Guldberg dan Waage
D. Mendeleev
E. Rutherford dan Bohr
2) Perhatikan pernyataan berikut :
1) dengan membentuk kation, caranya dengan melepas elektron valensi
2) dengan cara menangkap elektron dan menjadi ion positif
3) penggunaan bersama pasangan elektron
4) pembentukan anion dengan pelepasan elektron
Pernyataan yang benar dalam hubungannya dengan keadaan unsur dalam rangka mencapai konfigurasi elektron yang stabil adalah ... .
A. 1, 2, dan 3
B. 1 dan 3
C. 2 dan 4
D. 4 saja
E. 1, 2, 3, dan 4
3) Ikatan ion dapat terjadi antara atom yang nomor atomnya ... .
A. 10 dan 9
B. 12 dan 17
C. 6 dan 8
D. 16 dan 1
E. 1 dan 16
4) Perhatikan molekul berikut :
1) CO2
2) N2
3) O2
4) H2O
Jika nomor atom C, H, N dan O masingmasing 6, 1, 7, dan 8, molekul yang mengandung ikatan kovalen rangkap dua (ganda) adalah ... .
A. 1,2, dan 3
B. 1 dan 3
C. 2 dan 4
D. 4 saja
E. 1, 2, 3, dan 4
5) Hubungan nomor atom/ion dan jumlah elektron valensi yang benar adalah … .
|
| Tanda | Nomor | Jumlah |
| A. | Mg N3- | 12 7 | 8 2 6 3 8 |
6) Pasangan unsur berikut ini yang dapat
dapat membentuk ikatan kovalen
adalah ... .
A. 11Na dan 15P
B. 12Mg dan 19K
C. 15P dan 17Cl
D. 17Cl dan 19K
E. 19K dan 20Ca
7) Perhatikan sifat -sifat suatu senyawa berikut ini :
1) Pada suhu kamar berujud padat/kristal
2) Titik didih dan titik leburnya tinggi
3) Larut dalam air dan menghantarlistrik
Sifat-sifat di atas berlaku untuk senyawa ... .
A. CO2
B. H2O
C. CaCl2
D. HCl
E. NH3
8) Keelektronegatifan unsur-unsur F, Cl, Br, dan I, masing-masing adalah 4, 3, 2, 8, dan 2,5. Senyawa di bawah ini yang kepolarannya paling kecil adalah ... .
A. F2
B. ICl
C. IBr
D. FBr
E. PCl
9) Atom 15X dengan atom 17Y dapat membentuk molekul XY3 maka pernyataan yang paling benar adalah ... .
A. atom pusat X mempunyai sepasang elektron bebas
B. bentuk molekul XY3 adalah trigonal planar
C. atom pusat X mempunyai tiga pasang elektron terikat
D. molekul XY bersifat polar
E. XY3 termasuk senyawa kovalen
10) Sebuah atom netral X mempunai konfigurasi elektron : 2, 8, 7. Jika unsur tersebut membentuk senyawa hidrida, maka senyawa yang terbentuk tersebut kemungkinannya adalah ... .
A. ionik denganl rumus XH2
B. ionik dengan rumus XH
C. kovalen dengan rumus XH2
D. kovalen dengan rumus XH
E. kovaJen dengan rumus XH3
11) Diketahui elektron valensi atom H = 1 ; O = 6; S = 6 ; N = 5 ; C = 4 , dan perhatikan molekul berikut:
1) H2O
2) NH3
3) CO2
4) SO2
Molekul yang di dalamnya mengandung ikatan kovalen koordinasi adalah ... .
A. 1,2, dan 3
B. 1 dan 3
C. 2 dan 4
D. 4 saja
E. 1, 2, 3, dan 4
12) Molekul di bawah ini yang momen dipolnya tidak sama dengan nol adalah … .
A. CH4 (no. atom H=1)
B. CO2 (no. atom C=6, O=8)
C. HCl (no. atom Cl=17)
D. BF3 (no. atom B=5; F=9)
E. BeCl2 (no. atom Be=4)
13) Senyawa berikut yang tidak mengikuti
kaidah okted adalah … .
A. CHCl3
B. NH3
C. H2O
D. CH4
E. PCl5
14) Untuk molekul biner, kepolaran
senyawa dapat ditentukan dari … .
A. jari-jari atomnya
B. jenis atomnya
C. muatannya
D. elektron valensinya
E. massa. atonmya
15) Molekul H2O memiliki domain elektron sebanyak … .
A. 1
B. 2
C. 3
D. 4
E. 5
16) Unsur P (nomor atom 15) bersenyawa dengan unsur Cl (nomor atom 17) membentuk PCl3. Banyaknya domain elektron bebas pada atom pusat dalam senyawa PCl3 adalah … .
A. 0
B. 1
C. 2
D. 3
E. 4
17) Jika atom pusat dinyatakan dengan A, domain elektron ikatan dengan X dan domain elektron bebas dengan E, manakah di antara molekul berikut yang tergolong tipe AX4E?
A. CO2
B. NH3
C. SCl4
D. XeF4
E. IF3
18) Jika nomor atom O = 8 dan nomor atom H = 1, maka tipe molekul dari H2O adalah ... .
A. AX2
B. AX2E
C. AX2E2
D. AX3E
E. AX4
19) Atom pusat dalam molekul NH3 mengalami hibridisasi ... .
A. sp
B. sp2
C. sp3
D. sp3d
E. sp3d2
20) Pasangan tipe hibridisasi dan bentuk molekul berikut yang benar adalah ... .
| Tipe | Bentuk molekul | |
| A. | sp | tetra hedron |
21) Bentuk molekul PCl5 adalah … .
A. bentuk – T
B. trigonal bipiramidal
C. tetrahedral
D. linier
E. segi empat datar
22) Sudut ikatan dalam molekul H2O adalah 104,5o lebih kecil dari sudut tetrahedral 109,5o. Hal itu terjadi karena … .
A. dalam molekul air terdapat 4 pasang elektron yang ekuivalen
B. gaya tolak pasangan elektron bebas > pasangan elektron ikatan
C. gaya tolak pasangan elektron bebas = pasangan elektron ikatan
D. gaya tolak pasangan elektron bebas < pasangan elektron ikatan
E. molekul H2O bersifat non polar
23) Dari senyawa berikut yang mempunyai ikatan kovalen dan bersifat polar adalah … .
1) H2O
2) BeCl2
3) HCl
4) BF3
24) Empat unsur M, N, Q, dan R dengan nomor atom berturut-turut 6, 11, 17, dan 19. Pasangan unsur yang dapat membentuk ikatan kovalen dan senyawa bersifat non polar adalah … .
A. M dan R
B. N dan R
C. N dan Q
D. M dan Q
E. Q dan R
25) Molekul berikut yang bersifat dipol permanen adalah … .
A. BeCl2
B. BF3
C. CCl4
D. PCl3
E. CH4
26) Keelektronegatifan atom-atom F, Cl, Br dan I berturut-turut adalah 4,0; 3,0; 2,8 dan 2,5. Molekul berikut yang paling polar adalah … .
A. FCl
B. IBr
C. FBr
D. F2
E. ICl
27) Ikatan Van der Waals terjadi … .
A. antar molekul atom non logam
B. antar molekul kovalen
C. antar molekul non polar
D. antar molekul yang sangat polar
E. antar molekul yang berbeda muatan
28) Senyawa yang dapat membentuk ikatan Van der Waals adalah … .
A. NH3
B. H2O
C. HF
D. CH4
E. KCl
29) Titik didih gas nitrogen lebih tinggi dibanding gas hidrogen sebab … .
A. nomor atom nitrogen lebih tinggi
B. massa molekul gas hidrogen lebih tinggi
C. ikatan Van der Waals nitrogen lebih kuat
D. ikatan Van der Waals hidrogen lebih kuat
E. gas hidrogen membentuk ikatan hidrogen
30) Senyawa manakah yang tidak membentuk ikatan hidrogen antar molekulnya?
A. CH3CHO
B. CH3OH
C. CH3NH2
D. NH3
E. HF
31) Diberikan pasangan kelompok senyawa berikut:
1. H2O dengan HCl
2. PH3 dengan HBr
3. NH3 dengan H2S
4. HF dengan H2O
5. NH3 dengan HF
Kelompok senyawa yang mempunyai ikatan hidrogen adalah … .
A. 1 dan 2
A. 2 dan 3
B. 3 dan 4
C. 4 dan 5
D. 5 dan 1
32) Jika keelektronegatifan H, Br, dan F masing-masing 2,1; 2,8; dan 4,0, manakah deret senyawa di bawah ini yang tersusun dengan urutan kepolaran yang menurun?
A. BrF, HF, HBr
B. HF, BrF, HBr
C. BrF, HBr, HF
D. HBr, HF, BrF
E. HBr, BrF, HF
33) Diberikan data sebagai berikut :
| Zat cair | Tekanan uap jenuh (mmHg) |
| P R | 20 35 56 112 224 |
Gaya tarik-menarik antarmolekul yang paling kuat terdapat dalam zat cair ... .
A. P
B. Q
C. R
D. S
E. T
34) Unsur P (nomor atom 15) bersenyawa dengan unsur Cl (nomor atom 17) membentuk PCl3. Banyaknya pasangan elektron bebas pada atom pusat dalam senyawa PCl3 adalah ... .
A. 0
B. 1
C. 2
D. 3
E. 4

Newest Blog
2025-6-3 / Admin / 998
Genza Info
Selamat dan Sukses untuk siswa Genza yang lolos PTN 2025, Suatu Bukti Akurasi sistem G-Consult Genza Education
Daftar nama siswa Genza Education yang berhasil lolos seleksi SNPMB 2025:
2026-05-31 18:23:28 / Ratih Puspasari, S.Pd, CtHt, CT / 998
genzainfo
Bagaimana Otak Kita Belajar? Rahasia Di Balik Otak Reptil, Mamalia, Dan Neokorteks
Melalui teori Triune Brain (Tiga Lapisan Otak) yang dicetuskan oleh neurosaintis Paul MacLean, kita diajak untuk memahami bahwa otak manusia tidak bekerja sebagai satu kesatuan tunggal yang kaku. Otak kita berevolusi dalam tiga lapisan utama: Otak Reptil (Batang Otak), Otak Mamalia (Sistem Limbik), dan Otak Neokorteks.
2026-03-12 12:19:05 / Admin / 998
Genza Info
DIBUKA PENERIMAAN TARUNA AKPOL BINTARA TAMTAMA POLRI 2026
Penerimaan terpadu anggota Polri Tahun Anggaran 2026 resmi dibuka bagi putra-putri terbaik bangsa yang ingin mengabdi sebagai pelindung, pengayom, dan pelayan masyarakat. Proses rekrutmen ini dilaksanakan secara nasional dengan prinsip BETAH (Bersih, Transparan, Akuntabel, dan Humanis.
2026-03-02 15:39:23 / Admin / 998
Genza info
GENZA TANJUNG PHM NOOR TAMPIL BERSAMA SANGGAR LANGIT TABALONG DALAM LOMBA BACA PUITISASI AL-QURAN
Genza Education Tanjung PHM Noor turut ambil bagian dalam kegiatan Lomba Membaca Puitisasi Al-Qur’an yang diselenggarakan pada hari ini, Sabtu (28/02/2026), bekerja sama dengan Sanggar Langit Tabalong
 Genza Education
Genza Education